|
|
| ||
| Геном человека содержит значительное количество потенциально опасных протоонкогенов, которые в результате небольших перестроек ДНК в соматических клетках могут превращаться в онкогены.
Часто они кодируют белки, участвующие в регуляции клеточного деления. Что неудивительно, ведь раковые клетки отличаются от нормальных именно способностью к постоянному росту и делению. Это сближает их со стволовыми клетками, в том числе и с надеждой регенеративной медицины — индуцированными плюрипотентными стволовыми клетками (ИПСК): самым простым и действенным способом их получения является повышение экспрессии определенного набора генов, включающего протоонкогены c-Myc и Klf4*. Для того чтобы безобидный и нужный организму протоонкоген превратился в зловредный онкоген, повышающий вероятность опухолевого перерождения, порой бывает достаточно всего одного события, называемого активацией протоонкогена. Чаще всего активация состоит в резком повышении уровня экспрессии гена. Достоверно установлены следующие механизмы активации протоонкогенов (рис. 1):
* — «Биомолекула» уже не раз публиковала материалы об ИПСК и способах их получения: «Была клетка простая, стала стволовая» [1], «Снежный ком проблем с плюрипотентностью» [2] и «Предохранитель ИПСК» [3]. — Ред.
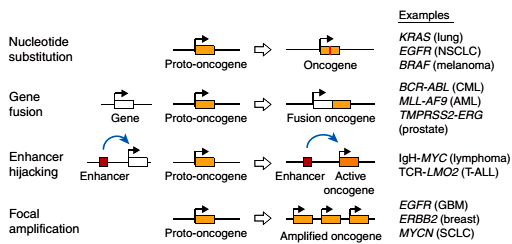 Рисунок 1. Известные механизмы активации протоонкогенов. Сверху вниз: нуклеотидная замена, слияние генов, захват энхансера, амплификация гена. Справа приведены примеры опухолей, в которых зарегистрирован тот или иной механизм активации протоонкогена. Рисунок из [8]. Рисунок 1. Известные механизмы активации протоонкогенов. Сверху вниз: нуклеотидная замена, слияние генов, захват энхансера, амплификация гена. Справа приведены примеры опухолей, в которых зарегистрирован тот или иной механизм активации протоонкогена. Рисунок из [8].Инсуляторные последовательности узнает специальный белок CTCF — важнейший фактор пространственной организации хроматина. Две молекулы CTCF способны связываться друг с другом, образуя таким образом петлю ДНК, ограниченную инсуляторами. Если энхансер и промотор располагаются в пределах одной такой петли, они взаимодействуют, если же они разделены сайтом связывания CTCF, энхансер теряет способность активировать данный промотор. Эти петли по-английски называются insulated neighborhoods («изолированные районы») [5], и в их состав суммарно может входить половина всей ДНК клетки (см. заглавный рисунок и рис. 2)! Получается, что именно от CTCF зависит, какие энхансеры с какими промоторами взаимодействуют. Роль CTCF в организации хроматина настолько важна, что инверсия (разворот на 180 градусов) участка ДНК, с которым он связывается, ведет к изменению топологии петель и нарушениям регуляции экспрессии генов [6]. 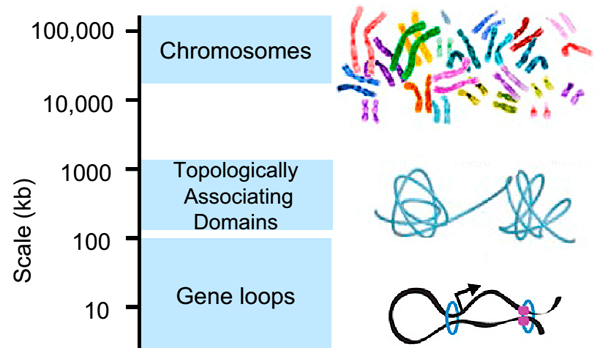 Рисунок 2. Современные представления об уровнях организации хроматина. Хромосомы составлены из так называемых топологически ассоциированных доменов (клубков хроматина), в состав которых входят петли. Видно, что крупная петля (insulated neighborhood), образованная белками CTCF (показан фиолетовым) и когезином (голубое кольцо), включает в себя петлю, образованную только когезином. Рисунок из [5]. Рисунок 2. Современные представления об уровнях организации хроматина. Хромосомы составлены из так называемых топологически ассоциированных доменов (клубков хроматина), в состав которых входят петли. Видно, что крупная петля (insulated neighborhood), образованная белками CTCF (показан фиолетовым) и когезином (голубое кольцо), включает в себя петлю, образованную только когезином. Рисунок из [5].Молекулярные биологи из нескольких лабораторий США решили выяснить, могут ли мутации в сайтах связывания CTCF приводить к активации протоонкогенов [8]. Для этого они проанализировали относительное расположение петель, образованных CTCF и когезином, и активированных онкогенов в хроматине клеток, происходящих из Т-клеточной лимфомы. Оказалось, что большинство изученных онкогенов (40 из 55) находились в пределах этих петель. 27 таких онкогенов активно экспрессировались, а из них 13 располагались в петлях, содержащих суперэнхансеры — группы близко расположенных друг к другу энхансеров. Сравнив геномы раковых и нормальных клеток, ученые выяснили, что в ряде случаев повышение экспрессии протоонкогена сопровождается делецией фрагмента ДНК, содержащего ближайший сайт связывания CTCF. Вероятно, в этих случаях граница петли перемещается, и в ее составе оказывается энхансер, что и приводит к активации протоонкогена. Чтобы подтвердить свою гипотезу, исследователи решили не искать уже существующие делеции, а получить их самостоятельно в ДНК Т-лимфоцитов. Любой приличный молекулярный биолог, решивший в наши дни получить геномную делецию, первым делом подумает про систему CRISPR/CAS9*. Авторы обсуждаемой статьи так и сделали: с помощью CRISPR/CAS9 они удаляли отдельные сайты связывания CTCF, раздвигая тем самым границы петель, и затем с удовольствием наблюдали за повышением уровня экспрессии протоонкогенов (рис. 3). Оказалось, что интенсивность контактов между участками ДНК, в норме находящимися в петле и за ее пределами, возросла. Эти данные свидетельствуют о том, что белок CTCF, изолируя протоонкогены от энхансеров, защищает их от активации.
* — Об этой системе и ее применении можно прочитать в статьях «CRISPR-системы: иммунизация прокариот» [9] и «Мутагенная цепная реакция: редактирование геномов на грани фантастики» [10]. — Ред.
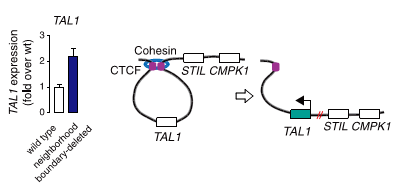 Рисунок 3. Активация протоонкогена TAL1 в результате делеции сайта связывания CTCF. В результате делеции, внесенной в геном с помощью CRISPR/CAS9 (показана красным), экспрессия протоонкогена TAL1 усилилась более чем в два раза (уровень экспрессии показан на гистограмме слева). Рисунок из [8]. Рисунок 3. Активация протоонкогена TAL1 в результате делеции сайта связывания CTCF. В результате делеции, внесенной в геном с помощью CRISPR/CAS9 (показана красным), экспрессия протоонкогена TAL1 усилилась более чем в два раза (уровень экспрессии показан на гистограмме слева). Рисунок из [8].Таким образом, новые данные дополнили наши представления о механизмах активации протоонкогенов. Эта информация может пригодиться как ученым, работающим над вопросами структурно-функциональной организации хроматина, так и онкологам. Последним, в частности, может быть интересна подмеченная авторами статьи особенность: описанный ими механизм активации протоонкогенов особенно активно используют клетки карцином пищевода и печени. В настоящее время ведутся дискуссии о возможностях терапии путем редактирования генома. «Биомолекула» сообщала о первых успешных опытах в этом направлении [11], но пока что использовался только метод относительно безопасного модифицирования клеток крови, которые затем удалялись из организма. Вмешиваться в геном клеток, которые останутся в организме пациента, — гораздо более рискованная задача. Тем не менее уже не за горами то время, когда редактирование ДНК будет введено в медицинскую практику. Чем больше мы к тому моменту узнаем о том, что именно нужно редактировать (например, устранять повреждения сайтов связывания CTCF в некоторых случаях рака), тем лучше. Литература
| |||
Темы
C
Cеквенирование
E
E1b1b
G
I
I1
I2
J
J1
J2
N
N1c
Q
R1a
R1b
Y-ДНК
Австролоиды
Альпийский тип
Америнды
Англия
Антропологическая реконструкция
Антропоэстетика
Арабы
Арменоиды
Армия Руси
Археология
Аудио
Аутосомы
Африканцы
Бактерии
Балканы
Венгрия
Вера
Видео
Вирусы
Вьетнам
Гаплогруппы
Генетика человека
Генетические классификации
Геногеография
Германцы
Гормоны
Графики
Греция
Группы крови
ДНК
Деградация
Демография в России
Дерматоглифика
Динарская раса
Дравиды
Древние цивилизации
Европа
Европейская антропология
Европейский генофонд
ЖЗЛ
Живопись
Животные
Звёзды кино
Здоровье
Знаменитости
Зодчество
Иберия
Индия
Индоарийцы
Интеръер
Иран
Ирландия
Испания
Исскуство
История
Италия
Кавказ
Канада
Карты
Кельты
Китай
Корея
Криминал
Культура Руси
Латинская Америка
Летописание
Лингвистика
Миграция
Мимикрия
Мифология
Модели
Монголоидная раса
Монголы
Мт-ДНК
Музыка для души
Мутация
Народные обычаи и традиции
Народонаселение
Народы России
Наши Города
Негроидная раса
Немцы
Нордиды
Одежда на Руси
Ориентальная раса
Основы Антропологии
Основы ДНК-генеалогии и популяционной генетики
Остбалты
Переднеазиатская раса
Пигментация
Политика
Польша
Понтиды
Прибалтика
Природа
Происхождение человека
Психология
РАСОЛОГИЯ
РНК
Разное
Русская Антропология
Русская антропоэстетика
Русская генетика
Русские поэты и писатели
Русский генофонд
Русь
США
Семиты
Скандинавы
Скифы и Сарматы
Славяне
Славянская генетика
Среднеазиаты
Средниземноморская раса
Схемы
Тохары
Тураниды
Туризм
Тюрки
Тюрская антропогенетика
Укрология
Уралоидный тип
Филиппины
Фильм
Финляндия
Фото
Франция
Храмы
Хромосомы
Художники России
Цыгане
Чехия
Чухонцы
Шотландия
Эстетика
Этнография
Этнопсихология
Юмор
Япония
генетика
интеллект
научные открытия
неандерталeц
Поиск по этому блогу
понедельник, 2 мая 2016 г.
Скрытая угроза: описан новый механизм активации протоонкогенов
Ярлыки:
Генетика человека,
ДНК